8th CMR Omnibus: ключові зміни у регулюванні косметичної продукції
Із наближенням ключової дати — 1 травня 2026 року — питання відповідності косметичної продукції новим вимогам ЄС набуває особливої актуальності. У статті зібрано основні положення 8-го CMR Omnibus та їх значення для ринку.
8-й пакет змін CMR Omnibus був опублікований у січні 2026 та передбачає оновлення Додатків II–V Регламенту ЄС про косметичну продукцію, таким чином вводячи нові заборони й обмеження для окремих інгредієнтів.
Станом на квітень 2026 року ЄС знаходиться у фінальній фазі підготовки до ключової дати — 1 травня 2026 року, після якої всі невідповідні продукти мають бути повністю вилучені з ринку ЄС.
У зв’язку з цим АПКУ інформує учасників ринку про ключові аспекти змін з метою підтримки належної підготовки та своєчасного реагування на нові регуляторні вимоги.
Annex II — Заборонені інгредієнти
- Sodium perborate та sodium peroxometaborate включені до одного запису (№1397).
- Silver (nano) [1nm<діаметр частинки≤100nm] та silver (massive) [діаметр частинки≥1mm] додані до Annex II, замінюючи попередній запис для колоїдного срібла (nano).
- Додано 15 нових речовин, з яких одна має INCI-назву: N,N’-methylenediacrylamide.
Annex III — Обмежені інгредієнти
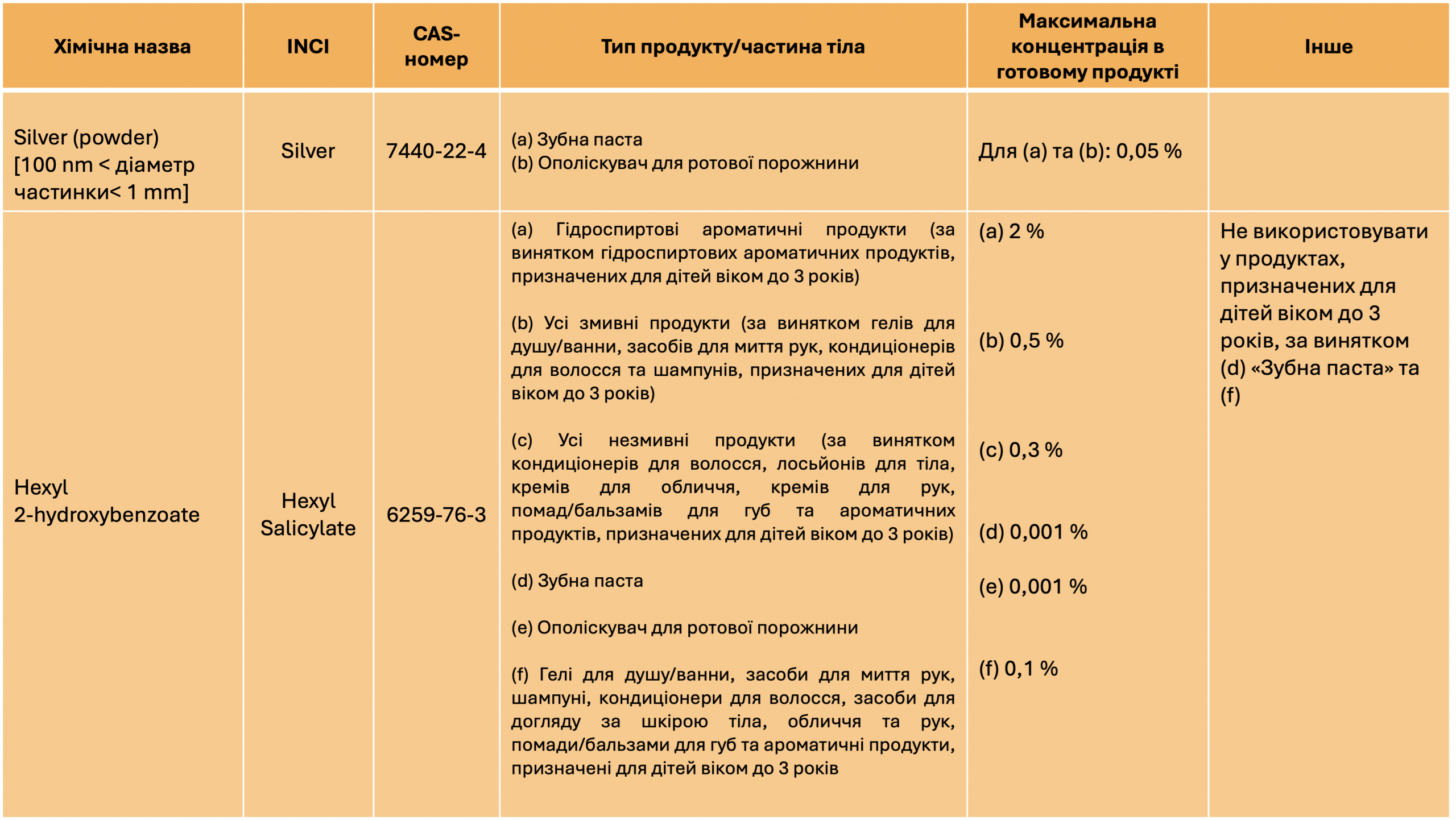
- Silver (powder) [100nm<діаметр частинки<1mm] — дозволено до 0,05% у зубних пастах та ополіскувачах для рота.
- Hexyl salicylate — встановлено диференційовані обмеження залежно від типу продукту та цільової аудиторії, зокрема:
- до 2% у гідроспиртових ароматах (крім продукції для дітей до 3 років);
- до 0,5% у змивних продуктах;
- до 0,3% у незмивних продуктах;
- до 0,001% у зубних пастах та ополіскувачах для рота;
- окремі, більш жорсткі обмеження для продукції, призначеної для дітей віком до 3 років.
Annex IV — Барвники, дозволені в косметиці
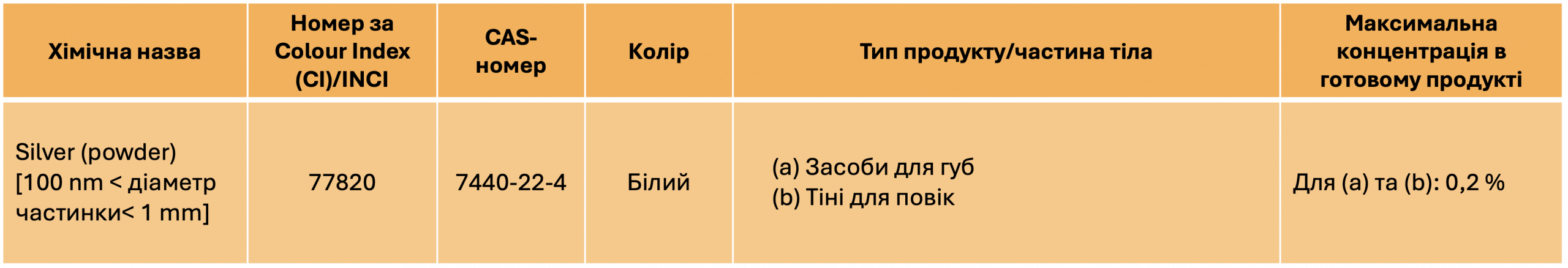
Silver (powder) [100nm<діаметр частинки<1mm] — дозволено до 0,2% у продуктах для губ та тінях для повік.
Annex V — Дозволені консерванти
- O-phenylphenol та sodium o-phenylphenate:
- до 0,2% (у перерахунку на фенол) у змивних продуктах;
- до 0,15% (у перерахунку на фенол) у незмивних продуктах.
- При комбінованому використанні сумарна концентрація не повинна перевищувати встановлені ліміти.
- Заборонено використання у:
- продуктах, що можуть призводити до інгаляційного впливу;
- продуктах для порожнини рота.
- Обов’язкове маркування: “Avoid contact with eyes”.

Дата застосування
8th CMR Omnibus набуде чинності з 1 травня 2026 року — це кінцева дата, до якої продукція може бути розміщена на ринку (off-shelf).
Що це означає для України?
Україна поступово імплементує підходи ЄС у сфері регулювання хімічної та косметичної продукції, і аналогічні вимоги з часом будуть інтегровані у національне законодавство. Це означає, що зміни, які сьогодні впроваджуються в Європейському Союзі, фактично формують майбутні правила гри і для українського ринку.
У цьому контексті Omnibus VIII є важливим сигналом для бізнесу: навіть якщо компанія наразі працює лише на внутрішньому ринку, підготовка до європейських вимог стає стратегічною необхідністю.
Для підготовки до нових вимог доцільно розпочати з практичних кроків:
- провести аудит складів продукції (INCI) на предмет наявності CMR-речовин або інгредієнтів, що підпадають під нові обмеження;
- перевірити відповідність сировини та отримати актуальну інформацію від постачальників щодо змін у класифікації речовин;
- оцінити необхідність reformulation для окремих продуктів;
- оновити технічну документацію;
- переглянути маркування з урахуванням можливих нових вимог;
- відстежувати подальші зміни у законодавстві ЄС та процес їх імплементації в Україні.





